医疗器械现场验收是保障设备安全、合规和有效使用的关键环节,需从资质核查、设备检验、性能测试、安全审查、报告编制与档案管理等多方面构建标准化流程体系。以下为具体验收要点:
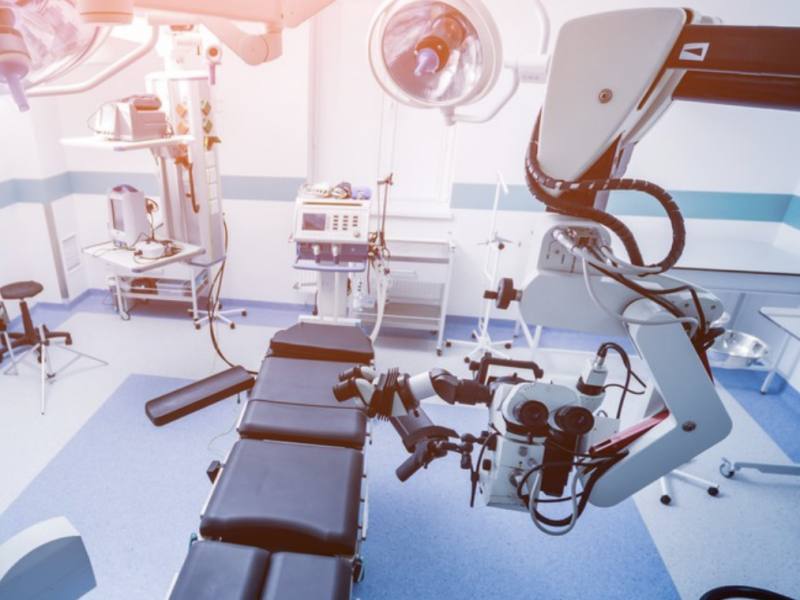
一、资质核查:确保设备合法合规
法定证照
核查《医疗器械注册证》《医疗器械生产许可证》《医疗器械经营许可证》等证件的真实性和有效期,重点核对设备型号、规格、生产日期是否与注册证一致。
进口设备需提供海关通关单、出入境检验检疫证明、CE/FDA认证(如适用)及中文说明书、标签。
示例:若缺少《医疗器械注册证》,设备可能属于非法流通产品,需立即终止验收。
合同与配置清单
逐项核对设备型号、配置、数量是否与采购合同完全一致,避免“货不对板”。
案例:某医院验收时发现设备配置低于合同约定,通过法律途径追回损失。
授权与售后
验证供应商的售后授权书、代理商资质及售后服务机构信息,确保后续服务有保障。
二、设备检验:从外观到功能的全面“体检”
包装与外观
检查外包装是否完好,核对序列号、报关单是否一致,防止运输损坏或“调包”。
观察设备表面是否有划痕、固定螺丝是否被开启过、按键是否灵活、通风口有无灰尘。
功能测试
基础功能:运行设备并对照技术参数,验证性能稳定性。例如,影像设备需测试分辨率,监护设备需模拟报警功能。
极端环境测试:模拟高温、高湿、电磁干扰等极端条件,验证设备适应性。
连续运行测试:满负荷运行72小时(如监护仪持续监测模拟信号),记录死机或误报警次数。
性能检测
使用专业工具检测物理参数(如超声频率、X射线剂量),进行电气安全测试(漏电流≤0.1mA、接地电阻≤0.1Ω)及生化质控品校准。
示例:CT设备需通过模体检测图像质量,确保分辨率、伪影等指标达标。
三、安全审查:防范潜在风险
电气安全
检测接地电阻、绝缘电阻、漏电流是否符合标准(如GB 9706.1),避免触电风险。
机械安全
验证紧急停止功能、防护门联锁装置是否有效(如CT机舱门遇阻自动弹开)。
辐射防护
用辐射剂量仪检测机房外泄漏剂量(如DR设备操作位≤2.5μSv/h),确保符合国家标准。
软件安全
检查软件是否为正式授权版本,验证数据加密功能及备份恢复机制。
四、报告编制与档案管理:实现全生命周期追溯
验收报告
形成包含量化数据记录、问题整改闭环的正式报告,明确复验标准,并由验收小组全员签字确认。
档案归档
将采购合同、验收报告、资质文件、操作手册、维修记录等纳入设备技术档案,保存期限至设备报废后5年以上。
建立电子化档案库,支持快速检索与追溯。
信息录入
将设备数据同步至医院管理系统,便于后续维护与计量校准提醒。
五、后续跟踪与风险防控:降低长期故障率
定期性能评估
制定季度或年度性能评估计划,例如每季度检测设备精度,防止“带病运行”。
供应商评价
根据设备使用反馈,建立供应商黑名单或优选库,优先选择提供预防性维护服务的供应商。
廉政风险防控
杜绝验收环节的“回扣”问题,严格执行采购公开透明制度。
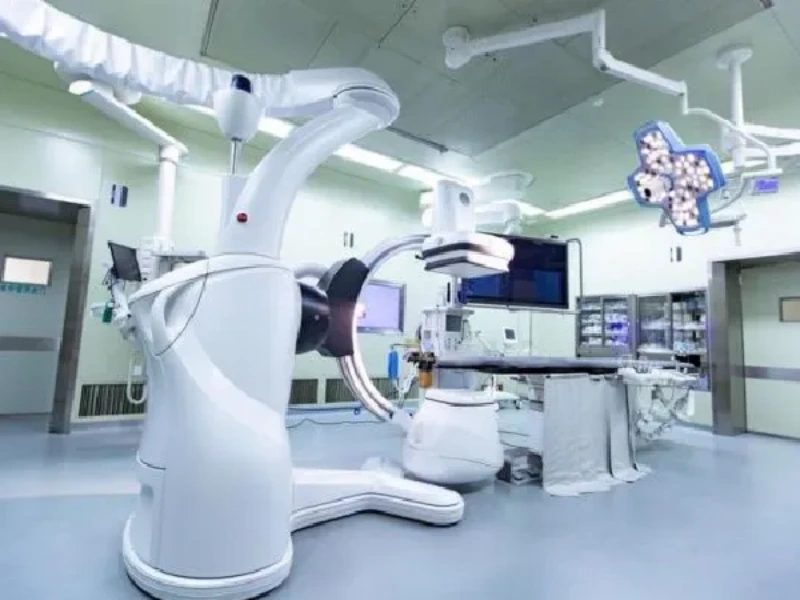
六、高风险设备附加要求
放射治疗设备
剂量输出误差≤±2%(如直线加速器),光野与照射野一致性≤±2mm,测试验证需第三方机构参与(如省级疾控中心)。
植入式器械
验证UDI(唯1设备标识)编码、灭菌证明、生物相容性报告,术后3个月随访率≥90%。
体外生命支持系统
血泵流量误差≤±5%,血浆分离效率≥95%,模拟紧急断电测试备用电源切换时间(≤10秒)。
相关推荐: