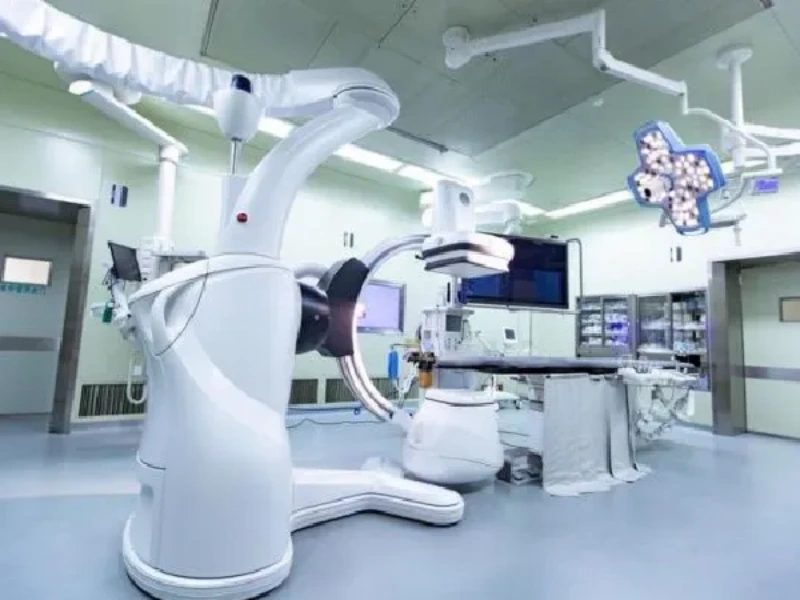
医疗有源设备检测是指对需要外部电源或内部电源(如电池)驱动的医疗器械进行性能、安全性和有效性的评估过程。这类设备通常涉及电能、光能、机械能等能量形式的输出(如心电图机、呼吸机、输液泵等),检测需严格遵循相关法规和标准。以下是关键要点:
1. 检测依据
• 国际标准:IEC 60601系列(电气安全与基本性能)、ISO 13485(质量管理体系)、ISO 14971(风险管理)。
• 中国法规:GB 9706.1(医用电气设备安全通用要求)、YY/T 1474(有源医疗器械可用性测试)等。
• 其他要求:FDA 21 CFR Part 820(美国)、EU MDR(欧盟)。
2. 检测内容
(1)电气安全检测
• 漏电流测试:患者漏电流、外壳漏电流(需符合GB 9706.1)。
• 绝缘电阻:高压下绝缘性能。
• 接地阻抗:保护接地连接的可靠性。
(2)性能检测
• 输出准确性:如呼吸机的潮气量、输液泵的流速误差。
• 环境适应性:温度、湿度、电磁兼容性(EMC,如辐射抗扰度、静电放电)。
• 软件验证:嵌入式软件的功能与网络安全(如IEC 62304)。
(3)生物相容性(接触患者时)
• 根据ISO 10993评估材料的安全性(如过敏、细胞毒性)。
(4)可用性与人因工程
• 操作界面设计是否避免误操作(参考IEC 62366)。
3. 检测流程
1. 设计阶段:风险分析(ISO 14971)、原型测试。
2. 型式检验:第三方检测机构按标准全面测试(如中国药监局认可的机构)。
3. 生产质量控制:批量生产时的抽样检测。
4. 上市后监督:不良事件监测与定期维护检测。
4. 常见问题与案例
• 案例1:某品牌输液泵因电磁干扰导致给药错误,需加强EMC测试。
• 案例2:呼吸机软件故障引发通气量异常,需强化软件验证。
5. 注意事项
• 认证要求:中国需取得NMPA注册证,欧盟需CE认证(MDR),美国需FDA 510(k)或PMA。
• 检测机构选择:需具备CNAS、CMA资质(如中国食品药品检定研究院)。
如需具体设备的检测方案或标准解读,可进一步说明设备类型(如影像类、治疗类等),以便提供针对性建议。
相关推荐: