
医疗器械验收机构是保障医疗设备质量与安全的核心环节,其专业性与权威性直接关系到患者诊疗效果和医疗机构运行安全。作为医疗器械进入临床使用的“守门人”,验收机构需通过资质审核、技术检测和流程监管,构建起覆盖全生命周期的质量管控体系。
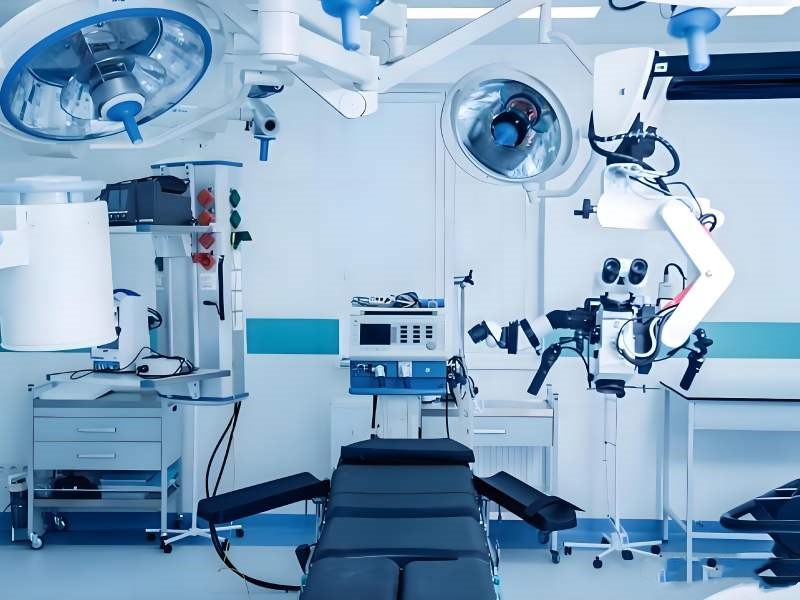
资质审核:严把准入门槛
验收机构需具备国家药监部门认定的医疗器械检验检测资质,涵盖有源设备、无源器械、体外诊断试剂等全类别检测能力。例如,对高风险植入物(如心脏支架)的验收,需核查生产企业的《医疗器械生产许可证》、产品注册证及生物相容性报告;对大型影像设备(如MRI),则需验证其电磁兼容性、辐射剂量等参数是否符合GB 9706系列标准。机构内部需建立专家库,涵盖临床医学、生物工程、计量校准等多领域人才,确保审核结论的科学性。
技术检测:量化指标
验收机构需配备高精度检测设备,如电气安全测试仪、辐射剂量计、光学性能分析系统等,对医疗器械的关键性能进行量化评估。例如,对呼吸机的验收需测试潮气量误差(≤±5%)、氧浓度稳定性(±3%以内);对体外诊断试剂的验收则需验证分析灵敏度、特异性及批间差等指标。检测过程需遵循ISO 17025实验室管理体系,确保数据可追溯、结果可复现。
流程监管:构建闭环管理
从到货开箱、安装调试到试运行验证,验收机构需全程监督并记录关键节点。例如,对冷链运输的生物制剂,需核查全程温度监控数据;对手术室设备,需模拟实际使用场景测试其抗干扰能力。验收完成后,机构需出具包含检测数据、结论及整改建议的正式报告,并建立电子档案长期留存。对于不合格设备,需联合监管部门启动追溯机制,防止问题产品流入市场。
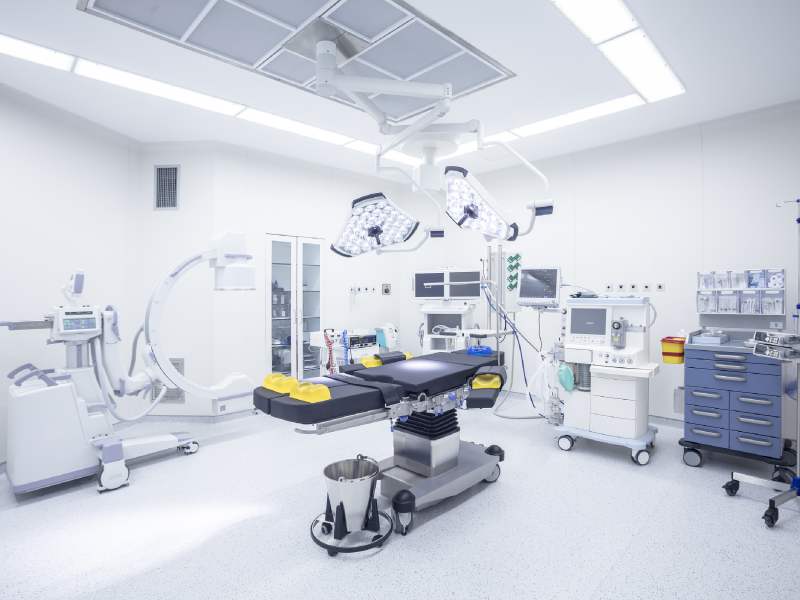
医疗器械验收机构通过专业化、标准化、闭环化的管理,为医疗安全构筑起坚实屏障,是推动医疗器械行业高质量发展的重要力量。
相关推荐: