医疗器械检验检测中心是保障医疗器械安全有效性的核心机构,其建设需遵循科学、规范、安全、高效的原则,涵盖选址规划、功能布局、设备配置、人员资质及管理体系五大核心要素。

选址与规划布局
中心应选址于工程地质稳定、市政基础设施完备、交通便利的地段,远离饮用水源保护区及化学、生物、电磁等污染源。总平面布局需充分利用地形,合理划分功能分区,实验用房宜置于楼宇上部,按毒理、理化、微生物实验室顺序由上至下排列,避免交叉干扰。机动车停车位数量需符合城乡规划要求,建筑密度不超过40%,绿地率宜达30%。
功能分区与实验室配置
实验室分为通用型(5类)和专业型(18类),按覆盖面、检验特殊性及时长分为一般、强化、特殊三类。通用型实验室涵盖物理性能、化学分析等基础检测,专业型实验室针对植入器械、电磁兼容等细分领域。例如,电磁兼容实验室需配备电波暗室,分子生物学实验室需配置PCR仪。实验室内部应划分清洁区、半污染区、污染区,设置缓冲间确保气流组织有效。
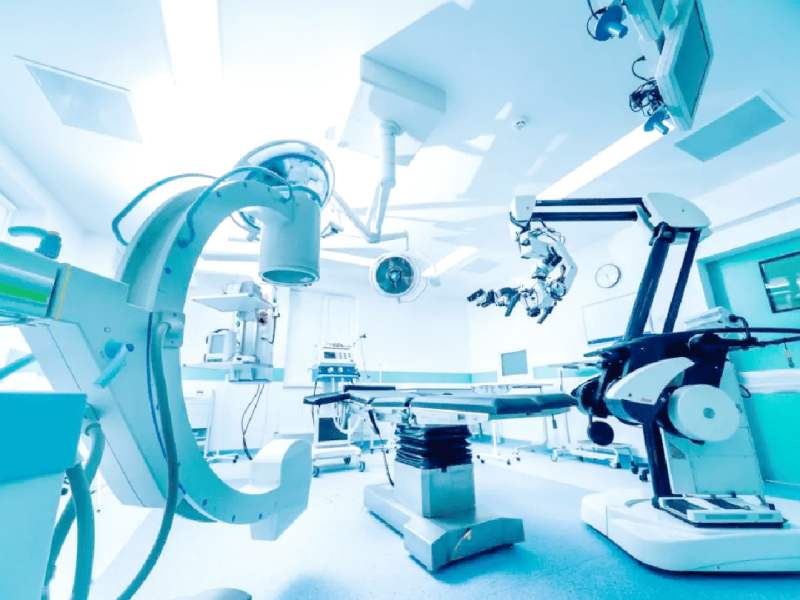
设备与仪器管理
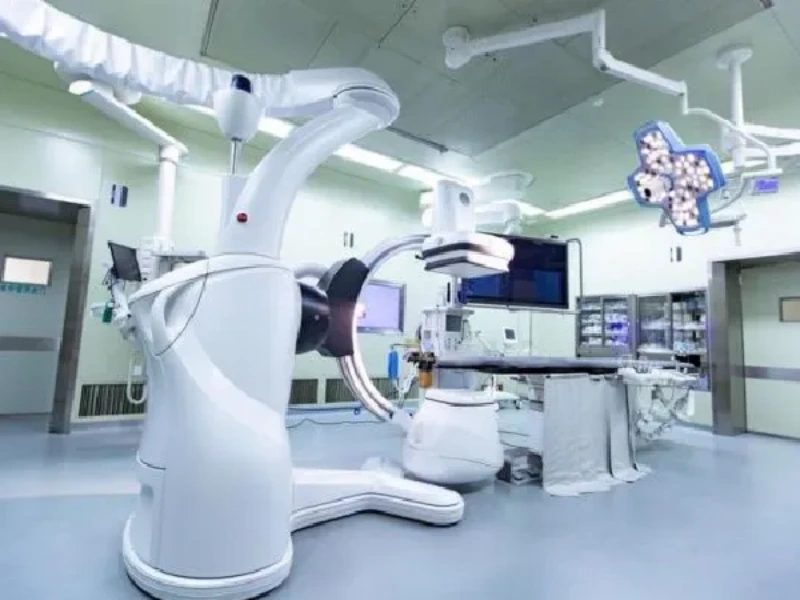
中心需配备生化分析仪、生物安全柜、恒温恒湿箱等基础设备,以及针对特定领域的专业设备。所有设备需定期校准维护,关键设备应配备不间断电源。设备选型需综合考虑尺寸、功率及环境要求,预留基础设施接口。
人员资质与团队建设
技术负责人需具备副高级以上职称或5年以上相关专业经验,检验人员中中级以上职称者占比不低于50%。操作人员需通过岗位技能考核,持证上岗。中心应建立人员培训档案,定期开展技术更新培训。
质量管理体系
中心需建立覆盖政策文件、操作程序、风险管理及安全规章制度的管理体系,并确保连续运行12个月以上。管理体系应通过内部审核和管理评审持续改进,同时参与外部质量评估计划,如实验室间比对,以验证检测能力。
相关推荐: