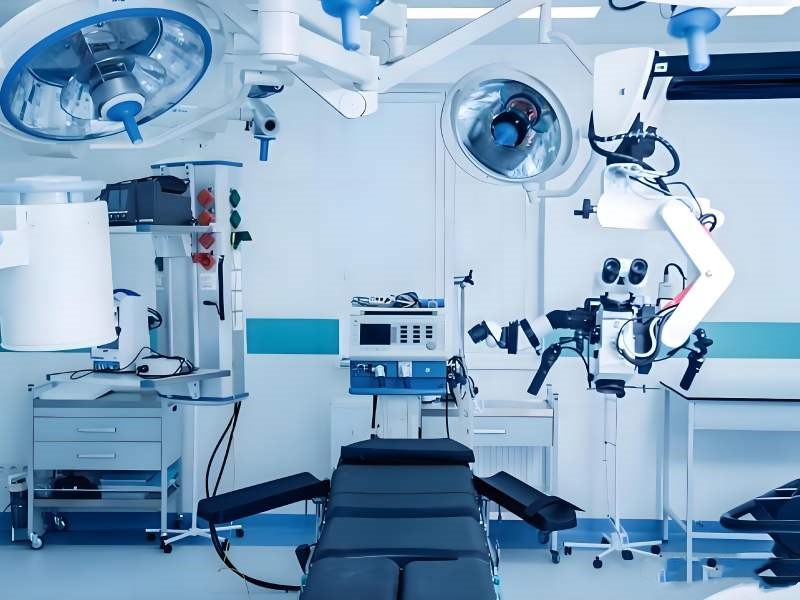
我们会根据您的IFU详细说明,验证您的医疗器械灭菌说明,这些步骤可以是湿热、低温过氧化氢或其他工艺。
适用标准
BS EN ISO 17664-1:2021 - 医疗产品加工。医疗器械制造商提供用于医疗器械加工的信息。关键及半关键医疗器械
ISO 14937:2009 - 医疗产品灭菌——灭菌剂特性及医疗器械
灭菌工艺的开发、验证和常规控制的一般要求 BS EN ISO 17665:2024 - 医疗产品灭菌。潮湿的热量。医疗器械灭菌工艺的开发、验证及常规控制要求。
灭菌过程
湿热(蒸汽-高压灭菌器)——这是一种利用高压蒸汽杀死医疗设备上微生物的灭菌技术。
低温过氧化氢灭菌——这是一种利用过氧化氢气体对热敏感医疗设备及其他设备的消毒工艺
生物指标——验证流程
生物指示剂用于验证灭菌过程。这些可以是标准的生物指示剂,例如孢子条或孢子悬浮液,可以直接在医疗设备上接种。生物指标应符合ISO 11138系列标准。
一种常见的部分循环验证灭菌过程的方法——基于过度设计方法,即在低于完整循环的条件下开发和验证工艺。该方法验证过程用于证明无菌保证水平(SAL)为12。
医疗器械灭菌验证
我们提供检测服务,确保您的医疗器械使用说明(IFU)中列出的灭菌说明已得到充分验证。根据ISO 17664《医疗产品加工:医疗器械制造商为医疗器械加工提供的信息》(第一部分为关键和半关键医疗器械,第二部分为非关键医疗器械),所有医疗器械制造商均有责任在器械再处理时提供使用指导。这些说明应经过全面验证,以确保设备的安全性。手动和自动(洗衣机消毒)工艺均应按照ISO 17664进行验证。